Jesteś tutaj
Восстановление фертильности женщин с помощью постнатальных тканей
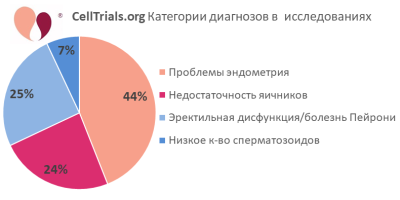
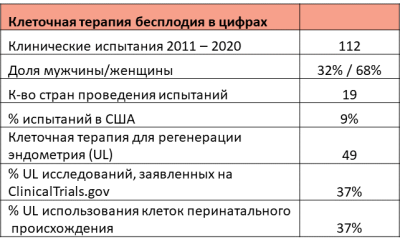 Клеточная терапия для восстановления фертильности - активная область исследований в некоторых странах. Доктор Вертер проанализировала 5695 клинических испытаний передовой клеточной терапии из базы данных CellTrials.org, охватывающих период с 2011 по 2020 годы, и извлекла 112 исследований, специально нацеленных на медицинские диагнозы, влияющие на фертильность. К мужским проблемам относятся: эректильная дисфункция, расстройство Пейрони и низкое количество сперматозоидов (азооспермия). Проблемы женщин касаются недостаточности яичников и множественных заболеваний слизистой оболочки матки (эндометрия), включая: тонкий эндометрий, неудачную имплантацию во время циклов вспомогательной репродукции, внутриматочные спайки и синдром Ашермана. Были исключены все заболевания мочевыводящих путей, мужские и женские.
Клеточная терапия для восстановления фертильности - активная область исследований в некоторых странах. Доктор Вертер проанализировала 5695 клинических испытаний передовой клеточной терапии из базы данных CellTrials.org, охватывающих период с 2011 по 2020 годы, и извлекла 112 исследований, специально нацеленных на медицинские диагнозы, влияющие на фертильность. К мужским проблемам относятся: эректильная дисфункция, расстройство Пейрони и низкое количество сперматозоидов (азооспермия). Проблемы женщин касаются недостаточности яичников и множественных заболеваний слизистой оболочки матки (эндометрия), включая: тонкий эндометрий, неудачную имплантацию во время циклов вспомогательной репродукции, внутриматочные спайки и синдром Ашермана. Были исключены все заболевания мочевыводящих путей, мужские и женские.
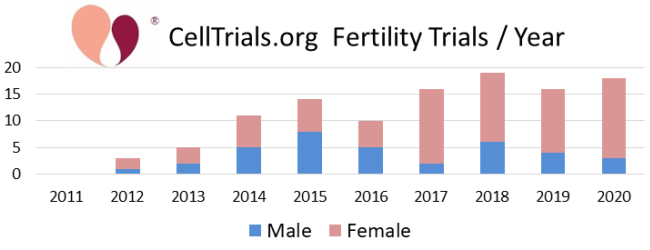
Первые два рисунка показывают, как полный набор из 112 исследований разбивается по количеству в год и долям, приходящим на основные диагностические категории.
 В этой статье мы сосредоточимся на 49 клинических испытаниях, зарегистрированных с 2011 по 2020 год, в которых использовалась клеточная терапия для регенерации эндометрия у бесплодных женщин. Эта область обязана своим появлением провокационной статье, опубликованной в 2004 году, в которой исследовались биопсии эндометрия у нескольких женщин, которые были реципиентами трансплантата костного мозга, и было обнаружено, что донорские клетки составляли почти половину эпителиальных клеток и стромальных клеток в их образцах биопсии¹. Последующие попытки повторить это исследование показали, что уровни донорских клеток ниже 10%², но энтузиазм по поводу регенерации эндометрия с помощью клеточной терапии был уже зарожден. Стволовые клетки, уникальные для эндометрия, были впервые идентифицированы в 2004 году и имеют потенциал в качестве инструмента регенеративной медицины³. На практике мы обнаружили, что на сегодняшний день только два клинических испытания утверждают, что стволовые клетки эндометрия использовались для лечения слизистой оболочки матки.
В этой статье мы сосредоточимся на 49 клинических испытаниях, зарегистрированных с 2011 по 2020 год, в которых использовалась клеточная терапия для регенерации эндометрия у бесплодных женщин. Эта область обязана своим появлением провокационной статье, опубликованной в 2004 году, в которой исследовались биопсии эндометрия у нескольких женщин, которые были реципиентами трансплантата костного мозга, и было обнаружено, что донорские клетки составляли почти половину эпителиальных клеток и стромальных клеток в их образцах биопсии¹. Последующие попытки повторить это исследование показали, что уровни донорских клеток ниже 10%², но энтузиазм по поводу регенерации эндометрия с помощью клеточной терапии был уже зарожден. Стволовые клетки, уникальные для эндометрия, были впервые идентифицированы в 2004 году и имеют потенциал в качестве инструмента регенеративной медицины³. На практике мы обнаружили, что на сегодняшний день только два клинических испытания утверждают, что стволовые клетки эндометрия использовались для лечения слизистой оболочки матки.
В 2011 году был опубликован новаторский клинический случай, в котором описывался успех клеточной терапии у женщины с синдромом Ашермана⁴. При синдроме Ашермана слизистая оболочка матки полностью замещена фиброзной тканью и спайками. От 2% до 22% бесплодных женщин страдают от внутриутробных спаек, с географическими вариациями в зависимости от частоты заболеваний и медицинской практики, которая может повредить эндометрий². Традиционное лечение синдрома Ашермана заключается в удалении спаек с помощью гистероскопии и последующей гормональной терапии. Однако около половины пациенток Ашермана не могут забеременеть после традиционной терапии⁵. Женщине в истории болезни 2011 года были имплантированы собственные стволовые клетки костного мозга в полость матки во время лечения бесплодия, и после этого вмешательства она смогла забеременеть⁴.
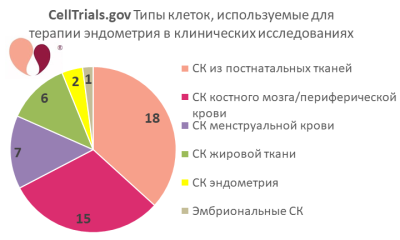 С тех пор ряд академических центров и клиник по лечению бесплодия включили клеточную терапию в методы лечения бесплодия для женщин с тонкой или рубцовой слизистой оболочкой матки. На второй круговой диаграмме показаны категории типов клеток, которые использовались в клинических испытаниях клеточной терапии слизистой оболочки матки. Средний целевой охват среди этих клинических испытаний составляет 76 женщин, с диапазоном от 10 до 500 пациентов. Обзор литературы и метаанализ, опубликованные в конце 2020 года, показали, что было опубликовано 8 статей с рецензией о контролируемых испытаниях клеточной терапии для лечения синдрома Ашермана⁵.
С тех пор ряд академических центров и клиник по лечению бесплодия включили клеточную терапию в методы лечения бесплодия для женщин с тонкой или рубцовой слизистой оболочкой матки. На второй круговой диаграмме показаны категории типов клеток, которые использовались в клинических испытаниях клеточной терапии слизистой оболочки матки. Средний целевой охват среди этих клинических испытаний составляет 76 женщин, с диапазоном от 10 до 500 пациентов. Обзор литературы и метаанализ, опубликованные в конце 2020 года, показали, что было опубликовано 8 статей с рецензией о контролируемых испытаниях клеточной терапии для лечения синдрома Ашермана⁵.
Клинические исследования показали, что имплантация стволовых клеток в матку увеличивает толщину эндометрия в статистически значимой степени5-14 и на длительный период времени14. Следовательно, терапия работает независимо от неполного объяснения механизма действия. Фактически, эффективность этой клеточной терапии намного превышает возможное приживление стволовых клеток, что приводит к аргументу, что паракринные эффекты должны играть доминирующую роль. Это было подтверждено группами, которые сравнивали экспрессию генов до и после биопсии.10,15
Однако в этой области предстоит еще многое сделать. Существуют огромные различия в точных методах, используемых в разных клинических испытаниях. Параметры, которые различаются между исследованиями, включают тип клеток, процессинг клеток, дозу клеток, сопутствующие лекарства и хирургические процедуры и т.д.
Большинство исследователей сходятся в цели трансплантации стволовых клеток в матку, которая состоит в том, чтобы они поселились в базальном слое эндометрия, но конкретные пути введения, используемые для доставки клеток, также широко варьируются в зависимости от клинических испытаний. Один из методов доставки - это вливание клеток в спиральные артериолы, которые представляют собой небольшие артерии, снабжающие кровью эндометрий. В большинстве исследований клетки вводят непосредственно в эндометрий во время гистероскопии. Более сложный метод, используемый в 11 из 49 клинических испытаний, заключается в загрузке клеток в какой-либо тип матрикса (обычно коллагеновый каркас), а затем трансплантация этого участка искусственно созданной ткани в слизистую оболочку матки.
В прошлом женщины с неизлечимым бесплодием часто обращались к суррогатным матерям, чтобы вынашивать беременность. Однако суррогатное материнство - очень дорогой вариант и сопряжен со многими юридическими и этическими сложностями. Все больше стран запрещают родителям нанимать коммерческих суррогатов16. В этих условиях исследования по восстановлению фертильности женщин приобретают новую актуальность. Клеточная терапия слизистой оболочки матки потенциально может быть менее затратной и более доступной, чем суррогатное материнство, если она может перейти от клинических испытаний к одобренным методам лечения, открытым для широкой публики14,16.
References
- Taylor HS. Endometrial cells derived from donor stem cells in bone marrow transplant recipients. JAMA 2004; 292(1):81–85.
- Gargett CE, Schwab KE, Deane JA. Endometrial stem/progenitor cells: the first 10 years. Human Reproduction Update 2016; 22(2):137–163.
- Chan RW, Schwab KE, Gargett CE. Clonogenicity of human endometrial epithelial and stromal cells. Biology of Reproduction 2004; 70(6):1738-1750.
- Nagori CB, Panchal SY, Patel H. Endometrial regeneration using autologous adult stem cells followed by conception by in vitro fertilization in a patient of severe Asherman's syndrome. J Human Reproductive Sciences 2011; 4(1):43-8. [cells from autologous bone marrow]
- Zhao Y, Luo Q, Zhang X, Qin Y, Hao J, Kong D, Wang H, Li G, Gu X, Wang H. Clinical Efficacy and Safety of Stem Cell-Based Therapy in Treating Asherman Syndrome: A System Review and Meta-Analysis. Stem Cells International 2020; 2020:8820538 [review & meta-analysis]
- Singh N, Mohanty S, Seth T, Shankar M, Dharmendra S, Bhaskaran S. Autologous stem cell transplantation in refractory Asherman's syndrome: a novel cell based therapy. J Human Reproductive Sciences 2014; 7(2):93–98. [cells from autologous bone marrow]
- Santamaria X, Cabanillas S, Cervelló I, Arbona C, Raga F, Ferro J, et al. Autologous cell therapy with CD133+bone marrow-derived stem cells for refractory Asherman's syndrome and endometrial atrophy: A pilot cohort study. Human Reproduction 2016; 31(5):1087–1096. [cells from autologous apheresis]
- Tan J, Li P, Wang Q, Li Y, Li X, Zhao D, Xu X, Kong L. Autologous menstrual blood-derived stromal cells transplantation for severe Asherman's syndrome. Human Reproduction 2016; 31(12):2723–2729. [cells from menstrual blood]
- Zhao G, Cao Y, Zhu X. et al. Transplantation of collagen scaffold with autologous bone marrow mononuclear cells promotes functional endometrium reconstruction via downregulating ΔNp63 expression in Asherman's syndrome. Science China Life Sciences 2017; 60(4):404–416. [cells from autologous bone marrow]
- Cao Y, Sun H, Zhu H. et al. Allogeneic cell therapy using umbilical cord MSCs on collagen scaffolds for patients with recurrent uterine adhesion: a phase I clinical trial. Stem Cell Research & Therapy 2018; 9:192 [umbilical cord MSC]
- Azizi R, Aghebati-Maleki L, Nouri M, Marofi F, Negargar S, Yousefi M. Stem cell therapy in Asherman syndrome and thin endometrium: Stem cell- based therapy. Biomedicine & Pharmacotherapy 2018; 102:333-343. [review]
- Lee SY, Shin JE, Kwon H, Choi DH, Kim JH. Effect of autologous adipose-derived stromal vascular fraction transplantation on endometrial regeneration in patients of Asherman's syndrome: a pilot study. Reproductive Sciences 2020; 27(2):561–568. [autologous adipose SVF]
- Ma H, Liu M, Li Y. et al. Intrauterine transplantation of autologous menstrual blood stem cells increases endometrial thickness and pregnancy potential in patients with refractory intrauterine adhesion. J Obstetrics Gynaecology Research 2020; 46(11):2347–2355. [cells from menstrual blood]
- Singh N, Shekhar B, Mohanty S, Kumar S, Seth T, Girish B. Autologous Bone Marrow-Derived Stem Cell Therapy for Asherman's Syndrome and Endometrial Atrophy: A 5-Year Follow-up Study. J Human Reproductive Sciences 2020; 13(1):31-37. [cells from autologous bone marrow]
- de Miguel-Gómez L, Ferrero H, López-Martínez S, Campo H, López-Pérez N, Faus A, Hervás D, Santamaría X, Pellicer A, Cervelló I. Stem cell paracrine actions in tissue regeneration and potential therapeutic effect in human endometrium: a retrospective study. BJOG 2019; 127(5):551-560.
- Bagri/Anand NT. A Controversial Ban on Commercial Surrogacy Could Leave Women in India With Even Fewer Choices. TIME Magazine Published 2021-06-30