Usted está aquí
Desinformación en el artículo del New York Times sobre el banco de sangre de cordón umbilical
El 15 de julio de 2024, el NYT publicó un artículo sobre el almacenamiento familiar de sangre de cordón umbilical que fue tan negativo que me veo obligado a escribir esta refutación. El NYT emplea a algunos de los mejores periodistas de investigación del mundo; soy suscriptora del NYT y lo leo todas las mañanas antes de comenzar mi día. Pero el trabajo de periodista les obliga a ser un ser un experto en todos los oficios y maestro en ninguno. En el curso de su apresurada investigación sobre el almacenamiento de sangre de cordón umbilical, los autores del artículo del NYT confundieron ciertos conceptos y optaron por la fácil salida de presentar la historia como un gran escándalo.
El artículo del NYT mostró las experiencias personales de cuatro familias que almacenaron la sangre de cordón de manera privada en los EE.UU., pero luego no pudieron usarla para tratar a sus hijos porque estaba contaminada. Sus historias son verdaderas, y cada una es desgarradora para las familias involucradas.
La mayor desinformación en el artículo del NYT es la afirmación de que, cuando los ensayos clínicos reciben unidades de sangre de cordón de bancos privados, “más de la mitad fueron rechazadas debido a células de baja calidad”. La redacción de esta afirmación puede llevar a los padres a creer que la mitad de las unidades de sangre de cordón almacenadas en bancos familiares están de alguna manera contaminadas. De hecho, cuando el equipo del Dr. Kurtzberg en el Centro Médico de Duke comenzó a estudiar la terapia con sangre de cordón para condiciones neurológicas, publicaron que la tasa de contaminación de las unidades almacenadas en bancos privados era del 7.6%1. La Dr. Kurtzberg ha compartido, más recientemente, que la tasa de contaminación ha sido aproximadamente del 10%. Estas unidades contaminadas no pueden ser utilizadas en el contexto de un ensayo clínico aprobado por la FDA, incluso si la contaminación es un microorganismo simple que podría ser fácilmente contrarrestado con antibióticos. Hay que tener en cuenta que el nacimiento difícilmente es un proceso estéril y los bancos familiares dependen de numerosos equipos de obstetricia en todo el país para realizar las recolecciones. Sería útil que los obstetras tuvieran más formación en las buenas prácticas para la recolección de la sangre de cordón.
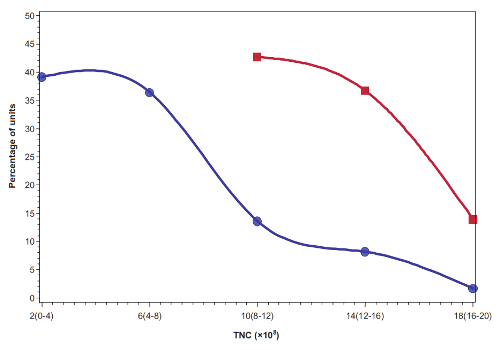
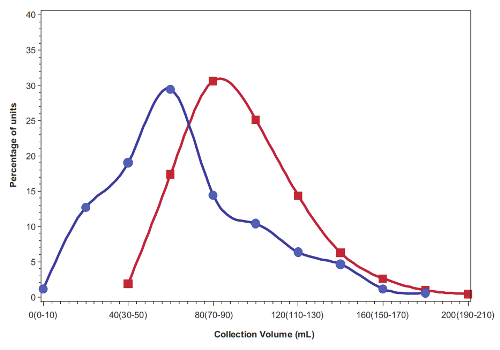
La principal razón por la que aproximadamente la mitad de las unidades de sangre de cordón de los bancos familiares son rechazadas en los ensayos clínicos es por su tamaño. Los ensayos clínicos actuales llevados a cabo por el equipo de la Dr. Kurtzberg requieren que cada niño reciba una dosis específica de células madre por kg de peso y muchas de las colecciones de sangre de cordón familiares son descalificadas porque no son lo suficientemente grandes para proporcionar esa dosis. La unidad mediana de sangre de cordón en los bancos familiares de EE.UU. tiene un volumen de 60 mL (2 onzas) y contiene 470 millones de células nucleadas totales (TNC)1. En comparación, los bancos públicos de sangre de cordón solo pueden permitirse conservar las muestras más grandes, las que tienen entre uno y dos mil millones de TNC, y pueden ser usadas para trasplantar a un adulto2. Por lo tanto, los bancos públicos de sangre de cordón desechan alrededor del 80% de las donaciones que reciben2. Dada esta información, los padres no deberían sentir que algo salió mal durante el parto si no obtuvieron una gran recolección de sangre de cordón, especialmente si hubo un pinzamiento tardío del cordón antes de la recolección. Los padres deben ser realistas sobre cuál es el tamaño normal de una recolección para el bebé promedio.
El elefante en la habitación que no fue discutido en el artículo del NYT es que cada uno de los padres decepcionados que entrevistaron estaba tratando de ingresar a su hijo en un ensayo clínico para tratar la parálisis cerebral o el autismo. No estaban tratando de obtener un tratamiento para una de las más de 80 enfermedades para las cuales la sangre de cordón es una terapia estándar y para las cuales se han realizado más de 45000 trasplantes de sangre de cordón en todo el mundo3. Así que indirectamente, el artículo del NYT ilustra cómo la sangre de cordón se ha convertido en un salvavidas de esperanza para los niños con trastornos neurológicos y cuán devastador es cuando no está disponible.
El NYT informó que “solo se han reportado 19 trasplantes de células madre usando la sangre de cordón del propio niño desde 2010, según el Centro de Investigación Internacional de Trasplante de Sangre y Médula Ósea” (CIBMTR). Lo que los autores del NYT no explicaron es que el CIBMTR solo mantiene registros de trasplantes de sangre de cordón para las más de 80 condiciones aprobadas, no rastrean las terapias de sangre de cordón en ensayos clínicos y programas de acceso expandido. Los tres bancos de sangre de cordón más grandes de EE.UU. han publicado listas de sus liberaciones de sangre de cordón para terapias4-6. Colectivamente, a finales de 2023, han permitido que más de 800 niños sean tratados con su propia sangre de cordón, y otros 590 niños han proporcionado tratamiento con sangre de cordón a un hermano4-6. Por lo tanto, aunque sigue siendo una tragedia que un pequeño número de familias no pudiera usar su sangre de cordón debido a la contaminación, ha habido más de 1300 familias que sí han usado su sangre de cordón almacenada de forma privada.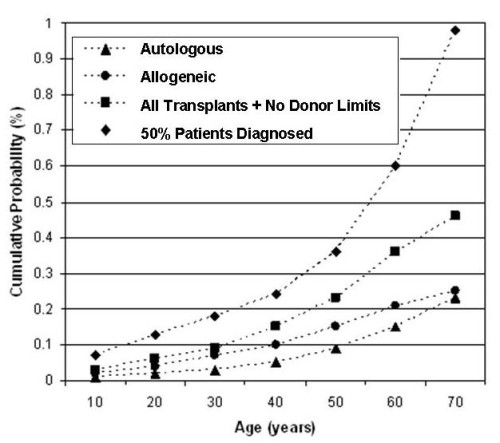 Fui citada por el NYT diciendo que la comercialización de la sangre de cordón para el trasplante de más de 80 enfermedades es una "exageración". Esta cita requiere algo de contexto. Primero, nuestro sitio web mantiene una lista de enfermedades tratables que incluye todas las enfermedades que pueden ser curadas por un trasplante de células madre. Segundo, la fuente del injerto para ese trasplante de células madre puede ser médula ósea, sangre periférica o sangre de cordón. La elección de la fuente de injerto la hace el médico que trata. No es una exageración decir que la sangre de cordón podría ser usada para cualquiera de estas enfermedades. Tercero, las probabilidades de que un niño tenga un trasplante de células madre por cualquier diagnóstico antes de los 20 años son solo 3 en 5.000 en los EE.UU7. Por eso dije que las posibilidades de que los niños usen sangre de cordón para cualquiera de las más de 80 enfermedades están siendo exageradas en la comercialización. Pero las probabilidades de que un niño necesite terapia con sangre de cordón para condiciones como nacimiento prematuro o parálisis cerebral son mucho más altas, y aquí es donde veo la motivación para el almacenamiento familiar.
Fui citada por el NYT diciendo que la comercialización de la sangre de cordón para el trasplante de más de 80 enfermedades es una "exageración". Esta cita requiere algo de contexto. Primero, nuestro sitio web mantiene una lista de enfermedades tratables que incluye todas las enfermedades que pueden ser curadas por un trasplante de células madre. Segundo, la fuente del injerto para ese trasplante de células madre puede ser médula ósea, sangre periférica o sangre de cordón. La elección de la fuente de injerto la hace el médico que trata. No es una exageración decir que la sangre de cordón podría ser usada para cualquiera de estas enfermedades. Tercero, las probabilidades de que un niño tenga un trasplante de células madre por cualquier diagnóstico antes de los 20 años son solo 3 en 5.000 en los EE.UU7. Por eso dije que las posibilidades de que los niños usen sangre de cordón para cualquiera de las más de 80 enfermedades están siendo exageradas en la comercialización. Pero las probabilidades de que un niño necesite terapia con sangre de cordón para condiciones como nacimiento prematuro o parálisis cerebral son mucho más altas, y aquí es donde veo la motivación para el almacenamiento familiar.
¡Es muy importante que los padres sepan que la lista de enfermedades raras varía según el país! La definición oficial de una enfermedad rara es aquella que afecta a menos de 60 por cada 100.000 personas en la población8. Dentro de los EE. UU., los trastornos sanguíneos hereditarios como la Enfermedad de Células Falciformes y la Talasemia están en la lista de enfermedades raras. En contraste, la Talasemia es común en países del Medio Oriente y Asia. Por ejemplo, en India, nacen 10.000 bebés cada año con una variante grave de Talasemia que requiere un trasplante de células madre para que el niño sobreviva9. Debido a la prevalencia de la Talasemia en su país, el almacenamiento de sangre de cordón es más importante como una forma de seguro biológico para los padres en India que para los padres en los EE. UU.
A lo largo de una vida de 70 años, la probabilidad de que una persona necesite un trasplante de células madre aumenta a al menos 1 en 2177. Esta estadística fue publicada en un artículo de 2008 por Nietfeld et al., y soy una de los coautores incluidos en el "et al." Mi amigo J.J. Nietfeld, PhD, que desde entonces se ha retirado, fue el autor que concibió ese estudio y lideró el esfuerzo para completarlo, no Mary Horowitz, MD, como se mencionó en el artículo del NYT. Calculamos las probabilidades de 1 en 217 de uso basándonos en la tasa a la que las personas se sometían a trasplantes de células madre (realizándolos, no solo necesitándolos) en los EE. UU. durante los años 2001-2003. La fracción de personas que se someten a trasplantes podría ser notablemente mayor ahora, dado el mayor acceso a los trasplantes en las últimas dos décadas, pero el cálculo no se ha repetido.
El artículo del NYT expuso algunas áreas donde los bancos familiares de sangre de cordón en los EE. UU. podrían y deberían practicar un mejor control de calidad. La FDA requiere que la sangre de cordón destinada al trasplante debe someterse a pruebas de esterilidad para verificar la contaminación microbiana o fúngica10. En los bancos públicos de sangre de cordón, cualquier unidad contaminada es desechada. En los bancos familiares de sangre de cordón, debido a que las muestras biológicas están destinadas a ser utilizadas en un entorno familiar, los bancos pueden conservar unidades contaminadas. Las dos agencias internacionales que acreditan los bancos de sangre de cordón, AABB y FACT, tienen protocolos para manejar y almacenar unidades contaminadas. Cuando las pruebas de esterilidad revelan contaminación, es justo y ético que se informe a los padres que están pagando por almacenar la sangre de cordón. Aparentemente, los bancos familiares de sangre de cordón no siempre hicieron esto en el pasado, según los testimonios en el artículo del NYT.
En conclusión, esta refutación fue necesaria para dejar claro que no es absolutamente cierto que aproximadamente la mitad de las unidades de sangre de cordón en los bancos familiares sean inútiles. Soy la fundadora y directora de la Parent’s Guide to Cord Blood Foundation (Fundación guía para padres sobre la sangre del cordón umbilical), una organización sin ánimo de lucro centrada en la educación de los padres y la defensa de los pacientes. Al escribir esta refutación, colaboré con la CBA (Asociación de Sangre de Cordón), una asociación profesional sin ánimo de lucro para bancos de sangre de cordón. Juntos, estamos emitiendo una llamada a la acción a la comunidad relacionada con la sangre de cordón: pedimos que los bancos familiares de sangre de cordón informen rutinariamente a los padres sobre el resultado de las pruebas de esterilidad en la muestra de sangre de cordón de su hijo.
References
- Sun J, Allison J, McLaughlin C, Sledge L, Waters-Pick B, Wease S, Kurtzberg J. Differences in quality between privately and publicly banked umbilical cord blood units: a pilot study of autologous cord blood infusion in children with acquired neurologic disorders. Transfusion. 2010; 50(9):1980-1987.
- Ciubotariu R. Timing of Umbilical Cord Clamping and Impact on Cord Blood Volume Collected for Banking. Parent's Guide to Cord Blood Foundation Newsletter Published 2016-12
- Ballen K. Update on umbilical cord blood transplantation. F1000Res. 2017; 6:1556.
- How some CBR families have used newborn stem cells. (handout)
- Viacord Cord Blood in Action
- Cryo-Cell Transplant/Infusion Matrix
- Nietfeld JJ, Pasquini MC, Logan BR, Verter F, Horowitz MM. Lifetime probabilities of hematopoietic stem cell transplantation in the U.S. Biol. Blood Marrow Transplant. 2008; 14(3):316-322.
- Crain E. What is a rare disease? Johnson & Johnson health & wellness blog. Published 2023-02-08
- Colah R, Italia K, Gorakshakar A. Burden of thalassemia in India: The road map for control. Pediatric Hematology Oncology 2017; 2(4):79-84.
- FDA Guidance for Industry. BLA for Minimally Manipulated, Unrelated Allogeneic Placental/Umbilical Cord Blood Intended for Hematopoietic and Immunologic Reconstitution in Patients with Disorders Affecting the Hematopoietic System. Food and Drug Administration Center for Biologics Evaluation and Research. Published March 2014. (see sterility testing on page 16)